Periodensystem der Elemente: Gruppen, Perioden und Blöcke
Eingeordnet in Chemie
Geschrieben am in  Deutsch mit einer Größe von 2,98 KB
Deutsch mit einer Größe von 2,98 KB
Gruppen im Periodensystem
Eine vertikale Spalte des Periodensystems wird als Gruppe bezeichnet. Alle Elemente, die zu einer Gruppe gehören, besitzen die gleiche Valenz und weisen daher ähnliche Merkmale oder Eigenschaften auf. Zum Beispiel haben Elemente der Gruppe IA eine Valenz von 1 (ein Elektron in ihrer äußersten Energieschale) und neigen dazu, dieses Elektron zu verlieren, um positive Ionen zu bilden. Die Elemente der letzten Gruppe auf der rechten Seite sind die Edelgase. Sie haben ihre äußerste Energieschale (Oktettregel) vollständig gefüllt und sind daher sehr reaktionsträge.
Von links nach rechts werden die Gruppen des Periodensystems der Elemente wie folgt bezeichnet:
- Gruppe 1 (IA): Die Alkalimetalle
- Gruppe 2 (IIA): Die Erdalkalimetalle
- Gruppe 3 (IIIB): Die Scandium-Gruppe
- Gruppe 4 (IVB): Die Titan-Gruppe
- Gruppe 5 (VB): Die Vanadium-Gruppe
- Gruppe 6 (VIB): Die Chrom-Gruppe
- Gruppe 7 (VIIB): Die Mangan-Gruppe
- Gruppe 8 (VIIIB): Die Eisen-Gruppe
- Gruppe 11 (IB): Die Kupfer-Gruppe
- Gruppe 12 (IIB): Die Zink-Gruppe
- Gruppe 13 (IIIA): Die Borgruppe
- Gruppe 14 (IVA): Die Kohlenstoffgruppe (Carbonoide)
- Gruppe 15 (VA): Die Stickstoffgruppe (Nitrogenoide)
- Gruppe 16 (VIA): Die Chalkogene
- Gruppe 17 (VIIA): Die Halogene
- Gruppe 18 (VIIIA): Die Edelgase
Perioden im Periodensystem
Die horizontalen Reihen des Periodensystems werden als Perioden bezeichnet. Im Gegensatz zu den Gruppen weisen die Elemente derselben Periode unterschiedliche chemische Eigenschaften auf, besitzen jedoch ähnliche Atomradien und Massen. Alle Elemente einer Periode haben die gleiche Anzahl von besetzten Elektronenschalen (Orbitalen). Jedes Element wird entsprechend seiner Elektronenkonfiguration platziert. Die erste Periode umfasst nur zwei Elemente: Wasserstoff und Helium, die beide nur das 1s-Orbital besitzen.
Blöcke im Periodensystem
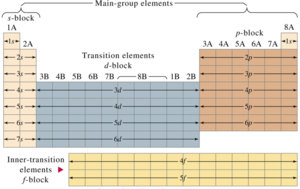
Das Periodensystem kann auch in Blöcke unterteilt werden, basierend auf den Orbitalen, die von den äußersten Elektronen besetzt werden.
Die Blöcke sind nach den Orbitalen benannt, die die äußersten Elektronen besetzen: s, p, d und f. Es könnten weitere Blöcke für andere Orbitale existieren, falls noch unentdeckte oder synthetisierte Elemente diese besetzen würden. In diesem Fall würden sie alphabetisch benannt werden.
